
¿QUÉ ES LA ZEOLITA?
La Zeolita es una roca compuesta de aluminio, silicio, y oxígeno. Se halla en una variedad de regiones del mundo donde la actividad volcánica prehistorica occurió cerca del agua, o donde el agua ha estado presente por milenios desde las erupciones. En 1756, el mineralogista sueco Baron Axel Fredrick Cronstedt descubrió la zeolita. Se relata que su perro sacó la piedra mientras escarbaba, y el mineralogista la llamó zeolita debido a que significa “perro” en sueco. En
otro relato, se dice que descubrió que cuando la zeolita (la cual era realmente Stilbite) se calentaba, emitía vapor. Zeolita significa “piedra hirviente” en griego. Como no sé sueco ni griego, tendrán que juzgar por su cuenta cual de estas historias son ciertas. Sabemos a ciencia cierta que la zeolita fue descubierta.
La zeolita tiene una porosidad natural debido a que tiene una estructura cristalina con ventanas, jaulas, y superjaulas. Las zeolitas naturales tienen ventanas de tamaño limitado (“tamaño de poro”) y todas son hidrofilicas (tienen afinidad por el agua). Algunas zeolitas sintéticas se parecen al carbón absorbente, dado que ambas pueden considerarse hidrofóbicas (tienen afinidad por los compuestos orgánicos, con poca o ninguna afinidad por el agua), y pueden adsorber vapores orgánicos con moleculas de tamaño más pequeño que el de sus poros. Tanto el carbón como la zeolita pueden adsorber agua y moleculas orgánicas; sin embargo, aquello por lo que tenga mayor afinidad, desplazará las demás moleculas. La zeolita tiene un “tamaño de poro”
uniforme, lo cual hace que se le denomine como un “tamiz molecular”, mientras parece que los carbones tienen poros que se comunican con poros más pequeños que a su vez se comunican con poros todavía más pequeños ad infinitum.
“El carbon absorbente”, el cual es en realidad un adsorbente, también tiene afinidad por el agua en algunos sitios, lo que disminuye su capacidad para adsorber las moleculas orgánicas de las corrientes que contienen moleculas de agua. Esto puede ser cierto o no en el caso de la zeolita, dependiendo del tipo de zeolita que se seleccione. Generalmente, entre mayor sea la razón de silicio y aluminio, más hidrofóbica es la zeolita. Las zeolitas hidrofóbicas tiene que ser sintetizadas, ya que no se encuentran en la naturaleza. ¡Por lo cual, la carrera para sintetizar
zeolitas con características específicas ha comenzado!
¿POR QUÉ SINTETIZAMOS LA ZEOLITA?
La sintesis es importante debido a que permite a los científicos e ingenieros
(1) predecir las propiedades de la zeolita,
(2) producir una zeolita con un “tamaño de poro” más grande, y
(3)producir zeolita hidrofóbica. Los intentos iniciales para sintetizar la zeolita simularon las condiciones volcánicas. Finalmente en 1949 se sintetizó la zeolita hidrofílica bajo condiciones hidrotérmicas (por ejemplo, a menos de 100 oC) por los químicos Milton, Breck, y otros investigadores. En 1985, los investigadores Bibby y Dale reportaron la síntesis de una zeolita de sílice pura. Otros investigadores han sintetizado una gran variedad de zeolitas hidrofilicas e hidrofóbicas.
Al sustituir otros elementos por aluminio o silica durante la síntesis, se han producido estructuras cristalinas como las de la zeolita, pero la zeolita de la que vamos a hablar aquí es un aluminosilicato puro.
Se han descubierto 40 zeolitas naturales; el Comité de Estructura de la Asociación Internacional de Zeolita ha catalogado 118 zeolitas; más de 600 zeolitas han sido identificadas, y si se incluyeran las estructuras cristalinas similares a las de las zeolitas (pero que utilizan otros elementos), el número aumentaría diariamente. Ninguna zeolita es exactamente igual a otra.
La estructura de un cristal de zeolita se basa en un tetrahedro que está formado por cuatro átomos de oxígeno enlazados con un átomo de silicio por medio de sus cuatro electrones de valencia. Estos tetrahedros se conectan en las “esquinas”de los oxígenos para formar los cristales.
Cuando el aluminio está presente durante la formación de los cristales, se sustituye el silicio por los átomos de aluminio, el cual tiene solamente tres electrones de valencia. El electrón de valencia que falta es proporcionado generalmente por un átomo de hidrógeno o de sodio debido a que estos elementos se encuentran típicamente en el agua hidratante. Esto distorciona el tetrahedro y hace un “sitio acído” para el intercambio de otros iones. Esto además hace que la estructura sea hidrofílica. Si la zeolita se forma en una mezcla que contenga un catión orgánico (por ejemplo, un
catión que tenga un núcleo de carbón), la estructura se puede formar alrededor del catión orgánico, utilizándolo como patrón. Esto a dado lugar a zeolitas hidrofílicas ricas en silicio con un “tamaño de poro” (o tamaño de ventana) lo suficientemente grande como para dejar pasar todo salvo las moléculas de petróleo que son más grandes.
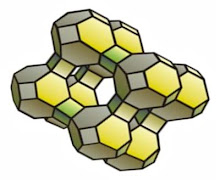
La estructura cristalina de una zeolita consiste de ventanas, jaulas, y superjaulas. Es por las ventanas que las moléculas llegan a las jaulas y superjaulas para ser adsorbidas o catalizadas. Las jaulas son las celdas más pequeñas en la estructura cristalina. Las superjaulas son las celdas dentro de la estructura cristalina que son más grandes que las jaulas y pueden incluso contener jaulas.
NIKOLAI DIAZ PASACHE



interesante, seria bueno si pusieran mas informacion tecnica, soy un estudiante de cali, colombia y estoy interesada en el tema
ResponderEliminarinteresante, me gustaria mas informacion de la parte quimica soy estudiante de ing. quimica en Cali, Colombia y estoy muy interesada gracis
ResponderEliminarEl hombre es grande y honrado cuando plantea tecnologia y que esta nos condusca al desarrollo humano en la interrelación con el cosmos y la acción de convivencia con el mundo. gracias apreciados hermanos por la Zeolita es alternativa de alta tecnologia, ppor favor siguan sosteniendo y desarrollando.
ResponderEliminar